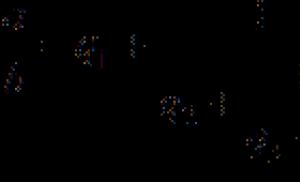ऑक्सीजन एक पदार्थ का विवरण है। ऑक्सीजन: तत्व के रासायनिक गुण। देखें कि "ऑक्सीजन" अन्य शब्दकोशों में क्या है
आक्सीजन आवर्त सारणी के पुराने लघु संस्करण के छठे-वें मुख्य समूह की दूसरी अवधि में है। नए नंबरिंग मानकों के मुताबिक यह 16वां ग्रुप है। संगत निर्णय IUPAC द्वारा 1988 में किया गया था। एक साधारण पदार्थ के रूप में ऑक्सीजन का सूत्र O2 है। इसके मुख्य गुणों, प्रकृति और अर्थव्यवस्था में भूमिका पर विचार करें। आइए ऑक्सीजन के नेतृत्व वाले पूरे समूह की विशेषताओं से शुरू करें। तत्व अपने संबंधित चाकोजेन्स से अलग है, और पानी हाइड्रोजन सेलेनियम और टेल्यूरियम से अलग है। परमाणु की संरचना और गुणों के बारे में जानकर ही सभी विशिष्ट विशेषताओं की व्याख्या की जा सकती है।
चाकोजेन्स ऑक्सीजन से संबंधित तत्व हैं।
समान गुणों वाले परमाणु आवर्त प्रणाली में एक समूह बनाते हैं। ऑक्सीजन चाकोजेन परिवार का प्रमुख है, लेकिन कई गुणों में उनसे भिन्न है।
समूह के पूर्वज ऑक्सीजन का परमाणु द्रव्यमान 16 एमू है। मी।हाइड्रोजन और धातुओं के साथ यौगिकों के निर्माण में चालकजन अपनी सामान्य ऑक्सीकरण स्थिति दिखाते हैं: -2। उदाहरण के लिए, पानी (H2O) की संरचना में, ऑक्सीजन की ऑक्सीकरण संख्या -2 है।
चाकोजेन्स के विशिष्ट हाइड्रोजन यौगिकों की संरचना सामान्य सूत्र से मेल खाती है: एच 2 आर। जब ये पदार्थ घुल जाते हैं, तो एसिड बनते हैं। केवल ऑक्सीजन के हाइड्रोजन यौगिक - पानी - में विशेष गुण होते हैं। वैज्ञानिकों के अनुसार यह असामान्य पदार्थ बहुत कमजोर अम्ल और बहुत कमजोर क्षार दोनों है।

सल्फर, सेलेनियम और टेल्यूरियम में ऑक्सीजन और अन्य उच्च इलेक्ट्रोनगेटिविटी (ईओ) गैर-धातु वाले यौगिकों में विशिष्ट सकारात्मक ऑक्सीकरण अवस्थाएं (+4, +6) होती हैं। चाकोजेन ऑक्साइड की संरचना सामान्य सूत्रों को दर्शाती है: RO2 , RO3 । संबंधित एसिड की संरचना है: एच 2 आरओ 3, एच 2 आरओ 4।
तत्व सरल पदार्थों के अनुरूप हैं: ऑक्सीजन, सल्फर, सेलेनियम, टेल्यूरियम और पोलोनियम। पहले तीन प्रतिनिधि गैर-धात्विक गुणों का प्रदर्शन करते हैं। ऑक्सीजन का सूत्र O2 है। उसी तत्व का एक एलोट्रोपिक संशोधन ओजोन (ओ 3) है। दोनों संशोधन गैस हैं। सल्फर और सेलेनियम ठोस अधातु हैं। टेल्यूरियम एक मेटलॉइड पदार्थ है, जो विद्युत प्रवाह का संवाहक है, पोलोनियम एक धातु है।
ऑक्सीजन सबसे आम तत्व है
हम पहले से ही जानते हैं कि एक ही रासायनिक तत्व का सरल पदार्थ के रूप में एक अन्य प्रकार का अस्तित्व होता है। यह ओजोन है, एक गैस जो पृथ्वी की सतह से लगभग 30 किमी की ऊंचाई पर एक परत बनाती है, जिसे अक्सर ओजोन स्क्रीन कहा जाता है। बाध्य ऑक्सीजन पानी के अणुओं में, कई चट्टानों और खनिजों, कार्बनिक यौगिकों की संरचना में शामिल है।

ऑक्सीजन परमाणु की संरचना
मेंडेलीव की आवर्त सारणी में ऑक्सीजन के बारे में पूरी जानकारी है:
- तत्व की क्रम संख्या 8 है।
- कोर चार्ज - +8।
- इलेक्ट्रॉनों की कुल संख्या 8 है।
- ऑक्सीजन का इलेक्ट्रॉनिक सूत्र 1s 2 2s 2 2p 4 है।
प्रकृति में, तीन स्थिर समस्थानिक हैं जिनकी आवर्त सारणी में समान क्रम संख्या है, प्रोटॉन और इलेक्ट्रॉनों की समान संरचना है, लेकिन न्यूट्रॉन की एक अलग संख्या है। समस्थानिकों को एक ही प्रतीक - O द्वारा निरूपित किया जाता है। तुलना के लिए, हम तीन ऑक्सीजन समस्थानिकों की संरचना को दर्शाते हुए एक आरेख प्रस्तुत करते हैं:

ऑक्सीजन के गुण - एक रासायनिक तत्व
परमाणु के 2p उपस्तर पर दो अयुग्मित इलेक्ट्रॉन होते हैं, जो ऑक्सीकरण अवस्थाओं -2 और +2 की उपस्थिति की व्याख्या करते हैं। सल्फर और अन्य चाकोजेन्स के साथ ऑक्सीकरण अवस्था को +4 तक बढ़ाने के लिए दो युग्मित इलेक्ट्रॉनों को अलग नहीं किया जा सकता है। इसका कारण एक मुक्त उपस्तर की अनुपस्थिति है। इसलिए, यौगिकों में रासायनिक तत्वऑक्सीजन लघु संस्करण में समूह संख्या के बराबर संयोजकता और ऑक्सीकरण अवस्था नहीं दिखाता है आवधिक प्रणाली(6)। इसकी सामान्य ऑक्सीकरण संख्या -2 है।
केवल फ्लोरीन वाले यौगिकों में ऑक्सीजन +2 की सकारात्मक ऑक्सीकरण स्थिति प्रदर्शित करता है, जो इसके लिए अनैच्छिक है। दो मजबूत गैर-धातुओं का ईओ मूल्य अलग है: ईओ (ओ) = 3.5; ईओ (एफ) = 4। एक अधिक विद्युतीय रासायनिक तत्व के रूप में, फ्लोरीन अपने इलेक्ट्रॉनों को अधिक मजबूती से रखता है और वैलेंस कणों को ऑक्सीजन परमाणुओं की ओर आकर्षित करता है। इसलिए, फ्लोरीन के साथ प्रतिक्रिया में, ऑक्सीजन एक कम करने वाला एजेंट है, यह इलेक्ट्रॉनों का दान करता है।

ऑक्सीजन एक साधारण पदार्थ है
1774 में अंग्रेजी शोधकर्ता डी। प्रिस्टले ने प्रयोगों के दौरान पारा ऑक्साइड के अपघटन के दौरान गैस जारी की। दो साल पहले, K. Scheele ने उसी पदार्थ को अपने शुद्ध रूप में प्राप्त किया। कुछ साल बाद ही, फ्रांसीसी रसायनज्ञ ए। लावोइसियर ने स्थापित किया कि किस तरह की गैस हवा का हिस्सा है, गुणों का अध्ययन किया। ऑक्सीजन का रासायनिक सूत्र O2 है। आइए हम पदार्थ की संरचना के रिकॉर्ड में एक गैर-ध्रुवीय सहसंयोजक बंधन - O :: O के निर्माण में शामिल इलेक्ट्रॉनों को दर्शाते हैं। आइए प्रत्येक बॉन्डिंग इलेक्ट्रॉन जोड़ी को एक लाइन से बदलें: O = O। यह ऑक्सीजन सूत्र स्पष्ट रूप से दर्शाता है कि अणु में परमाणु इलेक्ट्रॉनों के दो आम जोड़े के बीच जुड़े हुए हैं।

आइए सरल गणना करें और निर्धारित करें कि ऑक्सीजन का सापेक्ष आणविक भार क्या है: Mr (O 2) \u003d Ar (O) x 2 \u003d 16 x 2 \u003d 32। तुलना के लिए: Mr (वायु) \u003d 29। रासायनिक ऑक्सीजन का सूत्र एक ऑक्सीजन परमाणु से भिन्न होता है। इसका मतलब है कि श्रीमान (ओ 3) \u003d अर (ओ) x 3 \u003d 48। ओजोन ऑक्सीजन से 1.5 गुना भारी है।
भौतिक गुण
ऑक्सीजन एक रंगहीन, स्वादहीन और गंधहीन गैस है (सामान्य तापमान और वायुमंडलीय दबाव पर)। पदार्थ हवा से थोड़ा भारी है; पानी में घुलनशील, लेकिन कम मात्रा में। ऑक्सीजन का गलनांक ऋणात्मक होता है और -218.3 °C होता है। जिस बिंदु पर तरल ऑक्सीजन वापस गैसीय ऑक्सीजन में बदल जाती है, उसका क्वथनांक होता है। O2 अणुओं के लिए, इस भौतिक मात्रा का मान -182.96 ° C तक पहुँच जाता है। तरल और ठोस अवस्था में, ऑक्सीजन हल्का नीला रंग प्राप्त कर लेती है।
प्रयोगशाला में ऑक्सीजन प्राप्त करना
गर्म होने पर, ऑक्सीजन युक्त पदार्थ, जैसे पोटेशियम परमैंगनेट, एक रंगहीन गैस निकलती है, जिसे फ्लास्क या टेस्ट ट्यूब में एकत्र किया जा सकता है। यदि आप एक जलती हुई मशाल को शुद्ध ऑक्सीजन में लाते हैं, तो यह हवा की तुलना में अधिक चमक से जलती है। ऑक्सीजन प्राप्त करने के लिए दो अन्य प्रयोगशाला विधियां हाइड्रोजन पेरोक्साइड और पोटेशियम क्लोरेट (बर्थोलेट नमक) का अपघटन हैं। डिवाइस की योजना पर विचार करें, जिसका उपयोग थर्मल अपघटन के लिए किया जाता है।

एक टेस्ट ट्यूब या एक गोल-नीचे फ्लास्क में, थोड़ा सा बर्थोलेट नमक डालें, गैस आउटलेट ट्यूब के साथ एक डाट के साथ बंद करें। इसके विपरीत सिरे को (पानी के नीचे) उलटे फ्लास्क की ओर निर्देशित किया जाना चाहिए। गर्दन को पानी से भरे एक चौड़े गिलास या क्रिस्टलाइज़र में उतारा जाना चाहिए। जब बर्थोलेट नमक वाली परखनली को गर्म किया जाता है, तो ऑक्सीजन निकलती है। गैस आउटलेट ट्यूब के माध्यम से, यह पानी को विस्थापित करते हुए फ्लास्क में प्रवेश करता है। जब फ्लास्क को गैस से भर दिया जाता है, तो इसे पानी के नीचे एक कॉर्क से बंद कर दिया जाता है और पलट दिया जाता है। इस प्रयोगशाला प्रयोग में प्राप्त ऑक्सीजन का उपयोग एक साधारण पदार्थ के रासायनिक गुणों का अध्ययन करने के लिए किया जा सकता है।
दहन
यदि प्रयोगशाला पदार्थों को ऑक्सीजन में जला रही है, तो आपको अग्नि नियमों को जानने और उनका पालन करने की आवश्यकता है। हाइड्रोजन तुरंत हवा में जलती है, और ऑक्सीजन के साथ 2:1 के अनुपात में मिश्रित होती है, यह विस्फोटक है। शुद्ध ऑक्सीजन में पदार्थों का दहन हवा की तुलना में बहुत अधिक तीव्र होता है। इस घटना को वायु की संरचना द्वारा समझाया गया है। वायुमंडल में आक्सीजन का 1/5 भाग (21%) से थोड़ा अधिक है। दहन ऑक्सीजन के साथ पदार्थों की प्रतिक्रिया है, जिसके परिणामस्वरूप विभिन्न उत्पाद बनते हैं, मुख्य रूप से धातुओं और गैर-धातुओं के ऑक्साइड। दहनशील पदार्थों के साथ O2 का मिश्रण ज्वलनशील होता है, इसके अलावा, परिणामी यौगिक विषाक्त हो सकते हैं।
एक साधारण मोमबत्ती (या माचिस) का जलना कार्बन डाइऑक्साइड के निर्माण के साथ होता है। निम्नलिखित अनुभव घर पर किया जा सकता है। यदि आप किसी पदार्थ को कांच के जार या बड़े गिलास के नीचे जलाते हैं, तो जैसे ही सारी ऑक्सीजन खत्म हो जाएगी, दहन बंद हो जाएगा। नाइट्रोजन श्वसन और दहन का समर्थन नहीं करता है। ऑक्सीकरण का एक उत्पाद कार्बन डाइऑक्साइड अब ऑक्सीजन के साथ प्रतिक्रिया नहीं करता है। पारदर्शी आपको मोमबत्ती के जलने के बाद उपस्थिति का पता लगाने की अनुमति देता है। यदि दहन उत्पादों को कैल्शियम हाइड्रॉक्साइड के माध्यम से पारित किया जाता है, तो समाधान बादल बन जाता है। चूने के पानी और कार्बन डाइऑक्साइड के बीच एक रासायनिक प्रतिक्रिया होती है, जिसके परिणामस्वरूप अघुलनशील कैल्शियम कार्बोनेट बनता है।

औद्योगिक पैमाने पर ऑक्सीजन का उत्पादन
सबसे सस्ती प्रक्रिया, जिसके परिणामस्वरूप वायु मुक्त O2 अणु होते हैं, में रासायनिक प्रतिक्रियाएँ शामिल नहीं होती हैं। उद्योग में, कहते हैं, धातुकर्म संयंत्रों में, कम तापमान पर हवा और उच्च दबावद्रवीभूत करना। वायुमंडल के सबसे महत्वपूर्ण घटक, जैसे नाइट्रोजन और ऑक्सीजन, अलग-अलग तापमान पर उबलते हैं। सामान्य तापमान पर धीरे-धीरे गर्म करते हुए हवा के मिश्रण को अलग करें। पहले नाइट्रोजन के अणु निकलते हैं, फिर ऑक्सीजन। पृथक्करण विधि सरल पदार्थों के विभिन्न भौतिक गुणों पर आधारित है। ऑक्सीजन के एक सरल पदार्थ का सूत्र वही है जो वायु को ठंडा करने और द्रवीभूत करने से पहले था - O2.
कुछ इलेक्ट्रोलिसिस प्रतिक्रियाओं के परिणामस्वरूप, ऑक्सीजन भी जारी किया जाता है, इसे संबंधित इलेक्ट्रोड पर एकत्र किया जाता है। बड़ी मात्रा में औद्योगिक और निर्माण उद्यमों द्वारा गैस की आवश्यकता होती है। विशेष रूप से रासायनिक उद्योग में ऑक्सीजन की मांग लगातार बढ़ रही है। परिणामी गैस को चिह्नों के साथ प्रदान किए गए स्टील सिलेंडरों में औद्योगिक और चिकित्सा उद्देश्यों के लिए संग्रहीत किया जाता है। ऑक्सीजन वाले टैंकों को अन्य तरलीकृत गैसों - नाइट्रोजन, मीथेन, अमोनिया से अलग करने के लिए नीले या नीले रंग में रंगा जाता है।

O 2 अणुओं को शामिल करने वाली प्रतिक्रियाओं के सूत्र और समीकरणों के अनुसार रासायनिक गणना
अंकीय मूल्य दाढ़ जनऑक्सीजन एक अन्य मूल्य के साथ मेल खाता है - सापेक्ष आणविक भार। केवल पहले मामले में माप की इकाइयाँ हैं। संक्षेप में, ऑक्सीजन के पदार्थ और उसके दाढ़ द्रव्यमान का सूत्र निम्नानुसार लिखा जाना चाहिए: M (O 2) \u003d 32 g / mol। सामान्य परिस्थितियों में, किसी भी गैस का एक मोल 22.4 लीटर की मात्रा के बराबर होता है। इसका मतलब है कि 1 mol O2 एक पदार्थ का 22.4 लीटर है, 2 mol O2 44.8 लीटर है। ऑक्सीजन और हाइड्रोजन के बीच प्रतिक्रिया समीकरण के अनुसार, यह देखा जा सकता है कि हाइड्रोजन के 2 मोल और ऑक्सीजन के 1 मोल परस्पर क्रिया करते हैं:

यदि अभिक्रिया में 1 मोल हाइड्रोजन शामिल हो, तो ऑक्सीजन का आयतन 0.5 मोल होगा। 22.4 एल / मोल \u003d 11.2 एल।
प्रकृति और मानव जीवन में O2 अणुओं की भूमिका
पृथ्वी पर रहने वाले जीवों द्वारा ऑक्सीजन का उपभोग किया जाता है और यह पदार्थ के चक्र में 3 अरब से अधिक वर्षों से शामिल है। यह श्वसन और चयापचय के लिए मुख्य पदार्थ है, इसकी मदद से, पोषक अणु विघटित होते हैं, और जीवों के लिए आवश्यक ऊर्जा का संश्लेषण होता है। पृथ्वी पर लगातार ऑक्सीजन की खपत होती है, लेकिन प्रकाश संश्लेषण के माध्यम से इसके भंडार की भरपाई हो जाती है। रूसी वैज्ञानिक के. तिमिरयाज़ेव का मानना था कि इस प्रक्रिया के कारण हमारे ग्रह पर जीवन अभी भी मौजूद है।

प्रकृति और अर्थव्यवस्था में ऑक्सीजन की भूमिका महान है:
- जीवित जीवों द्वारा श्वसन की प्रक्रिया में अवशोषित;
- पौधों में प्रकाश संश्लेषण प्रतिक्रियाओं में भाग लेता है;
- कार्बनिक अणुओं का हिस्सा है;
- क्षय, किण्वन, जंग लगने की प्रक्रिया ऑक्सीजन की भागीदारी के साथ आगे बढ़ती है, जो ऑक्सीकरण एजेंट के रूप में कार्य करती है;
- कार्बनिक संश्लेषण के मूल्यवान उत्पाद प्राप्त करने के लिए उपयोग किया जाता है।
उच्च तापमान पर धातुओं को काटने और वेल्डिंग करने के लिए सिलेंडरों में तरलीकृत ऑक्सीजन का उपयोग किया जाता है। ये प्रक्रियाएँ मशीन-निर्माण संयंत्रों, परिवहन और निर्माण उद्यमों में की जाती हैं। पानी के नीचे, भूमिगत, उच्च ऊंचाई पर निर्वात में काम करने के लिए लोगों को O2 अणुओं की भी आवश्यकता होती है। बीमार लोगों द्वारा साँस ली जाने वाली हवा की संरचना को समृद्ध करने के लिए दवा में उपयोग किया जाता है। चिकित्सा प्रयोजनों के लिए गैस अशुद्धियों और गंध की लगभग पूर्ण अनुपस्थिति में तकनीकी गैस से भिन्न होती है।

ऑक्सीजन आदर्श ऑक्सीकरण एजेंट है
महान गैस परिवार के पहले प्रतिनिधियों को छोड़कर, आवर्त सारणी के सभी रासायनिक तत्वों के साथ ऑक्सीजन यौगिकों को जाना जाता है। हैलोजन, सोना और प्लेटिनम को छोड़कर कई पदार्थ सीधे ओ परमाणुओं के साथ प्रतिक्रिया करते हैं। बडा महत्वऑक्सीजन से जुड़ी घटनाएं होती हैं, जो प्रकाश और गर्मी की रिहाई के साथ होती हैं। ऐसी प्रक्रियाएं रोजमर्रा की जिंदगी और उद्योग में व्यापक रूप से उपयोग की जाती हैं। धातु विज्ञान में, ऑक्सीजन के साथ अयस्कों की परस्पर क्रिया को भूनना कहा जाता है। प्री-क्रश किए गए अयस्क को ऑक्सीजन युक्त हवा के साथ मिलाया जाता है। उच्च तापमान पर, धातु सल्फाइड से सरल पदार्थों में कम हो जाती है। इस प्रकार लोहा और कुछ अलौह धातुएँ प्राप्त होती हैं। शुद्ध ऑक्सीजन की उपस्थिति रसायन विज्ञान, प्रौद्योगिकी और धातु विज्ञान की विभिन्न शाखाओं में तकनीकी प्रक्रियाओं की गति को बढ़ाती है।
कम तापमान पर घटकों में अलग करके हवा से ऑक्सीजन प्राप्त करने की एक सस्ती विधि के उद्भव ने औद्योगिक उत्पादन के कई क्षेत्रों के विकास को प्रेरित किया। रसायनज्ञ O2 अणुओं और O परमाणुओं को आदर्श ऑक्सीकरण एजेंट मानते हैं। ये प्राकृतिक सामग्री हैं, वे प्रकृति में लगातार नवीनीकृत होते हैं, पर्यावरण को प्रदूषित नहीं करते हैं। इसके अलावा, ऑक्सीजन से जुड़ी रासायनिक प्रतिक्रियाएं अक्सर एक अन्य प्राकृतिक और सुरक्षित उत्पाद - पानी के संश्लेषण में समाप्त होती हैं। जहरीले औद्योगिक कचरे को बेअसर करने, प्रदूषण से पानी के शुद्धिकरण में O2 की भूमिका महान है। ऑक्सीजन के अलावा, इसके एलोट्रोपिक संशोधन, ओजोन का उपयोग कीटाणुशोधन के लिए किया जाता है। इस सरल पदार्थ में उच्च ऑक्सीकरण गतिविधि होती है। जब पानी का ओजोनीकरण किया जाता है, तो प्रदूषक विघटित हो जाते हैं। ओजोन का रोगजनक माइक्रोफ्लोरा पर भी हानिकारक प्रभाव पड़ता है।
>>
ऑक्सीजन के रासायनिक गुण। आक्साइड
यह पैराग्राफ इस बारे में है:
> सरल और के साथ ऑक्सीजन की प्रतिक्रियाओं के बारे में जटिल पदार्थ;
> यौगिक प्रतिक्रियाओं के बारे में;
> यौगिकों के बारे में जिन्हें ऑक्साइड कहा जाता है।
प्रत्येक पदार्थ के रासायनिक गुण प्रकट होते हैं रासायनिक प्रतिक्रिएंउसकी भागीदारी के साथ।
ऑक्सीजन सबसे सक्रिय गैर-धातुओं में से एक है। हो सामान्य परिस्थितियों में, यह कुछ पदार्थों के साथ प्रतिक्रिया करता है। बढ़ते तापमान के साथ इसकी प्रतिक्रियाशीलता काफी बढ़ जाती है।
सरल पदार्थों के साथ ऑक्सीजन की प्रतिक्रिया।
ऑक्सीजनप्रतिक्रिया, एक नियम के रूप में, गर्म होने पर, अधिकांश गैर-धातुओं और लगभग सभी धातुओं के साथ।
कोयले (कार्बन) के साथ प्रतिक्रिया। यह ज्ञात है कि कोयले को हवा में गर्म किया जाता है उच्च तापमान, रोशनी। यह ऑक्सीजन के साथ पदार्थ की रासायनिक प्रतिक्रिया की घटना को इंगित करता है। इस मामले में जारी होने वाली गर्मी का उपयोग, उदाहरण के लिए, ग्रामीण क्षेत्रों में घरों को गर्म करने के लिए किया जाता है।
कोयले के दहन का मुख्य उत्पाद कार्बन डाइऑक्साइड है। उसका रासायनिक सूत्र- सीओ 2। कोयला कई पदार्थों का मिश्रण है। इसमें कार्बन का द्रव्यमान अंश 80% से अधिक है। यह मानते हुए कि कोयले में केवल कार्बन परमाणु होते हैं, हम संबंधित रासायनिक समीकरण लिखते हैं:
टी
सी + ओ 2 \u003d सीओ 2।
कार्बन सरल पदार्थ बनाता है - ग्रेफाइट और हीरा। उनका एक सामान्य नाम है - कार्बन - और दिए गए रासायनिक समीकरण 1 के अनुसार गरम करने पर ऑक्सीजन के साथ परस्पर क्रिया करता है।
वे अभिक्रियाएँ जिनमें अनेक पदार्थों से एक पदार्थ का निर्माण होता है, यौगिक अभिक्रियाएँ कहलाती हैं।
सल्फर के साथ प्रतिक्रिया
यह रासायनिक परिवर्तन हर किसी के द्वारा किया जाता है जब वह माचिस की तीली पर प्रहार करता है; सल्फर इसके सिर का हिस्सा है। प्रयोगशाला में, ऑक्सीजन के साथ सल्फर की प्रतिक्रिया एक धूआं हुड में की जाती है। लोहे के चम्मच में थोड़ी मात्रा में सल्फर (हल्का पीला पाउडर या क्रिस्टल) गर्म किया जाता है। पदार्थपहले पिघलता है, फिर वायुमंडलीय ऑक्सीजन के साथ बातचीत के परिणामस्वरूप प्रज्वलित होता है और बमुश्किल ध्यान देने योग्य नीली लौ (चित्र 56, बी) के साथ जलता है। प्रतिक्रिया उत्पाद की तेज गंध है - सल्फर डाइऑक्साइड (माचिस जलाने के समय हम इस गंध को महसूस करते हैं)। सल्फर डाइऑक्साइड का रासायनिक सूत्र SO2 है, और प्रतिक्रिया समीकरण है
टी
एस + ओ 2 \u003d एसओ 2।
चावल। 56. सल्फर (ए) और हवा में इसका दहन (बी) और ऑक्सीजन में (सी)
1 ऑक्सीजन की अपर्याप्त मात्रा के साथ कार्बन का एक और यौगिक बनता है ऑक्सीजन- कार्बन मोनोआक्साइड
टी
सीओ: 2 सी + ओ 2 \u003d 2CO।

चावल। 57. लाल फास्फोरस (ए) और हवा में इसका दहन (बी) और ऑक्सीजन में (सी)
यदि जलते हुए सल्फर के साथ एक चम्मच ऑक्सीजन के साथ एक बर्तन में रखा जाता है, तो सल्फर हवा की तुलना में तेज लौ के साथ जलेगा (चित्र 56, सी)। इसे इस तथ्य से समझाया जा सकता है कि शुद्ध ऑक्सीजन में हवा की तुलना में अधिक O2 अणु होते हैं।
फास्फोरस के साथ प्रतिक्रिया। फास्फोरस, सल्फर की तरह, हवा की तुलना में ऑक्सीजन में अधिक तीव्रता से जलता है (चित्र 57)। प्रतिक्रिया उत्पाद सफेद है ठोस- फास्फोरस (\/) ऑक्साइड (इसके छोटे कण धुआं बनाते हैं):
टी
पी + ओ 2 -> पी 2 0 5।
प्रतिक्रिया योजना को रासायनिक समीकरण में बदलें।
मैग्नीशियम के साथ प्रतिक्रिया।
पहले, इस प्रतिक्रिया का इस्तेमाल किया गया था फोटोग्राफरचित्र लेते समय उज्ज्वल प्रकाश ("मैग्नीशियम फ्लैश") बनाने के लिए। रासायनिक प्रयोगशाला में, संबंधित अनुभव निम्नानुसार किया जाता है। मैग्नीशियम टेप को धातु चिमटी से लिया जाता है और हवा में आग लगा दी जाती है। चमकदार सफेद लौ के साथ मैग्नीशियम जलता है (चित्र 58, बी); आप इसे नहीं देख सकते! प्रतिक्रिया एक सफेद ठोस पैदा करती है। यह ऑक्सीजन के साथ मैग्नीशियम का एक यौगिक है; इसका नाम मैग्नीशियम ऑक्साइड है।

चावल। 58. मैग्नीशियम (ए) और हवा में इसका दहन (बी)
मैग्नीशियम की ऑक्सीजन के साथ अभिक्रिया के लिए एक समीकरण लिखिए।
जटिल पदार्थों के साथ ऑक्सीजन की प्रतिक्रिया। ऑक्सीजन कुछ ऑक्सीजन युक्त यौगिकों के साथ परस्पर क्रिया कर सकती है। उदाहरण के लिए, कार्बन मोनोऑक्साइड CO कार्बन डाइऑक्साइड बनाने के लिए हवा में जलती है:
टी
2CO + O 2 \u003d 2C0 2।
हम प्राकृतिक गैस (मीथेन), शराब, लकड़ी, कागज, मिट्टी के तेल आदि को जलाकर दैनिक जीवन में जटिल पदार्थों के साथ ऑक्सीजन की कई प्रतिक्रियाएँ करते हैं। जब इन्हें जलाया जाता है, तो कार्बन डाइऑक्साइड और जल वाष्प बनते हैं:
टी
सीएच 4 + 20 2 \u003d सीओ 2 + 2 एच 2 ओ;
मीथेन
टी
सी 2 एच 5 ओएच + 30 2 \u003d 2C0 2 + 3H 2 ओ।
अल्कोहल
आक्साइड।
पैराग्राफ में मानी जाने वाली सभी प्रतिक्रियाओं के उत्पाद ऑक्सीजन के साथ तत्वों के द्विआधारी यौगिक हैं।
दो तत्वों से बना यौगिक, जिनमें से एक ऑक्सीजन है, ऑक्साइड कहलाता है।
ऑक्साइड का सामान्य सूत्र EnOm है।
प्रत्येक ऑक्साइड का एक रासायनिक नाम होता है, और कुछ के पारंपरिक या तुच्छ 1 नाम भी होते हैं (तालिका 4)। ऑक्साइड का रासायनिक नाम दो शब्दों से मिलकर बना है। पहला शब्द संबंधित तत्व का नाम है, और दूसरा शब्द "ऑक्साइड" है। यदि किसी तत्व की संयोजकता परिवर्तनशील है, तो वह कई ऑक्साइड बना सकता है। उनके नाम अलग होने चाहिए। ऐसा करने के लिए, तत्व के नाम के बाद, कोष्ठक में एक रोमन अंक के साथ (बिना इंडेंटेशन के) ऑक्साइड में इसकी वैलेंस के मान को इंगित करें। एक यौगिक के लिए ऐसे नाम का एक उदाहरण क्यूप्रम (II) ऑक्साइड है ("क्यूप्रम-टू-ऑक्साइड" पढ़ें)।
तालिका 4

1 यह शब्द लैटिन शब्द ट्रिवियलिस - साधारण से आया है।
निष्कर्ष
ऑक्सीजन एक रासायनिक रूप से सक्रिय पदार्थ है। यह अधिकांश सरल पदार्थों के साथ-साथ जटिल पदार्थों के साथ भी संपर्क करता है। ऐसी प्रतिक्रियाओं के उत्पाद ऑक्सीजन - ऑक्साइड वाले तत्वों के यौगिक हैं।
वे अभिक्रियाएँ जिनमें अनेक पदार्थों से एक पदार्थ का निर्माण होता है, यौगिक अभिक्रियाएँ कहलाती हैं।
?
135. संयोजन और अपघटन की प्रतिक्रियाओं में क्या अंतर है?
136. प्रतिक्रिया योजनाओं को रासायनिक समीकरणों में बदलें:
ए) ली + ओ 2 -> ली 2 ओ;
एन 2 + ओ 2 -> नहीं;
बी) एसओ 2 + ओ 2 -> एसओ 3;
सीआरओ + ओ 2 -> सीआर 2 ओ 3।
137. दिए गए सूत्रों में से उन्हें चुनें जो ऑक्साइड के अनुरूप हों:
O2, NaOH, H2O, HCI, I2O5, FeO.
138. निम्नलिखित सूत्रों वाले ऑक्साइडों को रासायनिक नाम दें:
NO, Ti2 O 3, Cu 2 O, MnO 2, CI 2 O 7, V 2 O 5, CrO 3।
इस बात को ध्यान में रखें कि इन ऑक्साइड को बनाने वाले तत्वों की संयोजकता परिवर्तनशील होती है।
139. सूत्र लिखिए: क) प्लंबम(I\/) ऑक्साइड; बी) क्रोमियम (III) ऑक्साइड;
ग) क्लोरीन (आई) ऑक्साइड; डी) नाइट्रोजन (आई\/) ऑक्साइड; ई) ऑस्मियम (\/III) ऑक्साइड।
140. प्रतिक्रिया योजनाओं में सरल पदार्थों के सूत्र जोड़ें और रासायनिक समीकरण बनाएं:
ए) ... + ... -> सीएओ;
बी) नहीं + ... -> नहीं 2; ... + ... -> 2 ओ 3 के रूप में; एमएन 2 ओ 3 + ... -> एमएनओ 2।
141। उन प्रतिक्रिया समीकरणों को लिखें जिनके साथ आप परिवर्तनों की ऐसी "श्रृंखला" बना सकते हैं, अर्थात पहले पदार्थ से दूसरा और दूसरे से तीसरा प्राप्त करें:
ए) सी -> सीओ -> सीओ 2;
बी) पी -> पी 2 0 3 -> पी 2 0 5;
c) Cu -> Cu 2 O -> CuO।
142.. हवा में एसीटोन (सीएच 3) 2 सीओ और ईथर (सी 2 एच 5) 2 ओ के दहन के दौरान होने वाली प्रतिक्रियाओं के समीकरण बनाएं। प्रत्येक प्रतिक्रिया के उत्पाद कार्बन डाइऑक्साइड और पानी हैं।
143. ईओ 2 ऑक्साइड में ऑक्सीजन का द्रव्यमान अंश 26% है। तत्व ई परिभाषित करें।
144. दो फ्लास्क ऑक्सीजन से भरे हुए हैं। उनकी सीलिंग के बाद, अतिरिक्त मैग्नीशियम को एक फ्लास्क में जलाया गया, और अतिरिक्त सल्फर को दूसरे में जलाया गया। किस फ्लास्क में वैक्यूम होता है? उत्तर स्पष्ट कीजिए।
पोपेल पी.पी., क्रिकल्या एल.एस., रसायन विज्ञान: पड्रूच। 7 कोशिकाओं के लिए। zahalnosvit. nach. zakl. - के।: प्रदर्शनी केंद्र "अकादमी", 2008. - 136 पी .: आईएल।
पाठ सामग्री पाठ सारांश और समर्थन फ्रेम पाठ प्रस्तुति संवादात्मक प्रौद्योगिकियां शिक्षण विधियों को गति देती हैं अभ्यास प्रश्नोत्तरी, ऑनलाइन कार्यों का परीक्षण और कक्षा चर्चाओं के लिए गृहकार्य कार्यशालाओं और प्रशिक्षण प्रश्नों का अभ्यास करें रेखांकन वीडियो और ऑडियो सामग्री फोटो, चित्र ग्राफिक्स, टेबल, योजनाएं कॉमिक्स, दृष्टांत, कहावतें, वर्ग पहेली, उपाख्यान, चुटकुले, उद्धरण ऐड-ऑन जिज्ञासु लेख (MAN) साहित्य मुख्य और शब्दों की अतिरिक्त शब्दावली के लिए सार चीट शीट चिप्स पाठ्यपुस्तकों और पाठों में सुधार पाठ्यपुस्तक की त्रुटियों को सुधार कर पुराने ज्ञान को नए ज्ञान से बदलना केवल शिक्षकों के लिए कैलेंडर योजना प्रशिक्षण कार्यक्रम पद्धति संबंधी सिफारिशेंपरिचय
हर दिन हम उस हवा में सांस लेते हैं जिसकी हमें जरूरत होती है। क्या आपने कभी इस बारे में सोचा है कि अधिक सटीक रूप से, हवा में कौन से पदार्थ होते हैं? इसमें सबसे अधिक नाइट्रोजन (78%) होती है, इसके बाद ऑक्सीजन (21%) और अक्रिय गैसें (1%) होती हैं। हालांकि ऑक्सीजन हवा का सबसे बुनियादी हिस्सा नहीं है, इसके बिना वातावरण निर्जन होगा। उसके लिए धन्यवाद, पृथ्वी पर जीवन मौजूद है, क्योंकि नाइट्रोजन, एक साथ और व्यक्तिगत रूप से, मनुष्यों के लिए हानिकारक है। आइए ऑक्सीजन के गुणों को देखें।
ऑक्सीजन के भौतिक गुण
हवा में, ऑक्सीजन केवल अलग नहीं है, क्योंकि सामान्य परिस्थितियों में यह स्वाद, रंग और गंध के बिना गैस है। लेकिन ऑक्सीजन को एकत्रीकरण के अन्य राज्यों में कृत्रिम रूप से स्थानांतरित किया जा सकता है। तो, -183 o C पर यह तरल हो जाता है, और -219 o C पर यह कठोर हो जाता है। लेकिन ठोस और तरल ऑक्सीजन केवल मनुष्य ही प्राप्त कर सकता है, और प्रकृति में यह केवल गैसीय अवस्था में मौजूद है। ऐसा दिखता है (फोटो)। और बर्फ की तरह सख्त।
ऑक्सीजन के भौतिक गुण भी एक साधारण पदार्थ के अणु की संरचना हैं। ऑक्सीजन परमाणु दो ऐसे पदार्थ बनाते हैं: ऑक्सीजन (O2) और ओजोन (O3)। ऑक्सीजन अणु का मॉडल नीचे दिखाया गया है।

ऑक्सीजन। रासायनिक गुण
पहली चीज जिसके साथ किसी तत्व का रासायनिक लक्षण वर्णन शुरू होता है, वह डी। आई। मेंडेलीव में इसकी स्थिति है। तो, ऑक्सीजन मुख्य उपसमूह के 6 वें समूह की दूसरी अवधि में 8 नंबर पर है। इसका परमाणु द्रव्यमान 16 एमू है, यह एक अधातु है।
अकार्बनिक रसायन विज्ञान में, इसके द्विआधारी यौगिकों को अन्य तत्वों के साथ एक अलग एक-आक्साइड में जोड़ा गया था। ऑक्सीजन बन सकता है रासायनिक यौगिकधातु और अधातु दोनों।
आइए इसे प्रयोगशालाओं में प्राप्त करने के बारे में बात करते हैं।
रासायनिक रूप से, पोटेशियम परमैंगनेट, हाइड्रोजन पेरोक्साइड, बार्टोलेट नमक, नाइट्रेट्स को विघटित करके ऑक्सीजन प्राप्त किया जा सकता है सक्रिय धातुएँऔर भारी धातु ऑक्साइड। इन विधियों में से प्रत्येक के लिए प्रतिक्रिया समीकरणों पर विचार करें।
1. जल इलेक्ट्रोलिसिस:
एच 2 ओ 2 \u003d एच 2 ओ + ओ 2
5. भारी धातु ऑक्साइड (जैसे पारा ऑक्साइड) का अपघटन:
2HgO \u003d 2Hg + O 2
6. सक्रिय धातुओं के नाइट्रेट का अपघटन (उदाहरण के लिए, सोडियम नाइट्रेट):
2NaNO 3 \u003d 2NaNO 2 + O 2
ऑक्सीजन का अनुप्रयोग
हम रासायनिक गुणों के साथ कर रहे हैं। अब मानव जीवन में ऑक्सीजन के उपयोग के बारे में बात करने का समय आ गया है। विद्युत और ताप विद्युत संयंत्रों में ईंधन के दहन के लिए इसकी आवश्यकता होती है। यह वेल्डिंग और धातु काटने के लिए कच्चा लोहा और स्क्रैप धातु से स्टील का उत्पादन करने के लिए प्रयोग किया जाता है। अग्निशामकों के मुखौटे, गोताखोरों के सिलेंडरों के लिए ऑक्सीजन की आवश्यकता होती है, इसका उपयोग लौह और अलौह धातु विज्ञान में और विस्फोटकों के निर्माण में भी किया जाता है। खाद्य उद्योग में भी, ऑक्सीजन को खाद्य योज्य E948 के रूप में जाना जाता है। ऐसा लगता है कि कोई भी उद्योग ऐसा नहीं है जहाँ इसका उपयोग नहीं किया जाता है, लेकिन यह चिकित्सा में सबसे महत्वपूर्ण भूमिका निभाता है। वहां उन्हें "मेडिकल ऑक्सीजन" कहा जाता है। ऑक्सीजन प्रयोग करने योग्य होने के लिए, यह पूर्व-संपीड़ित है। ऑक्सीजन के भौतिक गुण इस तथ्य में योगदान करते हैं कि इसे संपीड़ित किया जा सकता है। इस रूप में, यह इनके समान सिलेंडरों के अंदर जमा होता है।

इसका उपयोग बीमार रोगी के शरीर में जीवन प्रक्रियाओं को बनाए रखने के साथ-साथ कुछ बीमारियों के उपचार में पुनर्वसन और उपकरणों में संचालन में किया जाता है: अपघटन, गैस्ट्रोइंटेस्टाइनल ट्रैक्ट की विकृतियां। इसकी मदद से डॉक्टर रोजाना कई लोगों की जान बचाते हैं। ऑक्सीजन के रासायनिक और भौतिक गुण इसके व्यापक उपयोग में योगदान करते हैं।
पाठ 1।
विषय। ऑक्सीजन ऑक्सीजन, इसके अणु की संरचना, भौतिक गुण।
प्रयोगशाला अपघटन प्रतिक्रिया में ऑक्सीजन प्राप्त करना।
एक उत्प्रेरक की अवधारणा।
पाठ मकसद: पाठ के दौरान छात्रों के रासायनिक ज्ञान को समेकित करने के लिए
ऑक्सीजन और के उदाहरण पर तत्व और सरल पदार्थ
ऑक्सीजन;
विचार करें कि प्रयोगशाला में ऑक्सीजन कैसे प्राप्त करें और
उद्योग;
छात्रों को ऑक्सीजन की खोज के इतिहास से परिचित कराना और
प्रकृति में ऑक्सीजन तत्व का वितरण;
वायु और उसके संघटन के बारे में विद्यार्थियों के ज्ञान का सामान्यीकरण कर सकेंगे;
अपघटन प्रतिक्रिया का एक विचार तैयार करें,
उत्प्रेरक।
अतिरिक्त के साथ काम करने की क्षमता विकसित करना जारी रखें
साहित्य, सामान्यीकरण, मुख्य बात पर प्रकाश डालें।
कक्षाओं के दौरान।
1. संगठन। पल।
2. छात्रों के बुनियादी ज्ञान को अद्यतन करना।
रसायन शास्त्र किसका अध्ययन करता है?
पदार्थ को परिभाषित कीजिए।
साधारण पदार्थ किसे कहते हैं? उदाहरण दो।
सरल पदार्थों को किन दो समूहों में बांटा गया है?
धातुओं और अधातुओं के उदाहरण दीजिए।
धातुएँ अधातुओं से कैसे भिन्न होती हैं?
एक "रासायनिक तत्व" क्या है?
"रासायनिक तत्व" और "सरल पदार्थ" में क्या अंतर है?
3. नई सामग्री सीखना।
इस पाठ से हम उन पदार्थों से परिचित होना शुरू करते हैं जो मानव जीवन में महत्वपूर्ण भूमिका निभाते हैं - इन पदार्थों में से एक ऑक्सीजन है।
ऑक्सीजन के बारे में आप पहले से क्या जानते हैं?
तुम और क्या जानना चाहोगे?
धार्मिक लोगों के अनुसार, केवल ईश्वर ही सर्वव्यापी, सर्वशक्तिमान और एक ही समय में अदृश्य हो सकता है। वास्तव में, ये तीनों विशेषण रासायनिक तत्व के लिए परमाणु संख्या 8 - ऑक्सीजन के साथ काफी संभव हैं, जो सरल पदार्थ ऑक्सीजन बनाता है।
सोचो और तालिकाओं में भरें - एक रासायनिक तत्व और एक साधारण पदार्थ की विशेषताएं।
रासायनिक संकेत सरल पदार्थ
तत्व का नाम ऑक्सीजन यौगिक सूत्रहे 2
प्रतीक मिस्टर 32
एआर 16 भौतिक गुण
वैलेंस 11 रासायनिक गुण
रसीद
प्रकृति में होना
आवेदन
आपको क्या लगता है कि ऑक्सीजन तत्व कहाँ पाया जाता है?
सुरक्षात्मक छाल के द्रव्यमान का 47%
(सीओ2, फ़े2 हे3, अल2 हे3 और टी . पी .)
65% शरीर का वजन
के बारे में 2
इंसान
80% जलमंडल ( एच 2 हे)
रासायनिक तत्व ऑक्सीजन ऐसी काव्य पंक्तियों का पात्र है।
मैं तुम्हें खरोंच रहा हूँ,
बो ऑक्सीजन - im "मैं मेरा हूँ।
मैं पेड़ों में, घास के पास हूं
तुम्हारी रगों में, तुम्हारे खून में।
साधारण पदार्थ ऑक्सीजन के भौतिक गुणों के बारे में हम क्या जानते हैं?
पर सामान्य परिस्थितियों में यह एक ऐसी गैस है जो रंगहीन, स्वादहीन और गंधहीन होती है। यह हवा से भारी होता है और हवा को विस्थापित करके एकत्र किया जाता है। यह पानी में थोड़ा घुलनशील है, लेकिन यह जीवित प्राणियों (मछली, कीड़े आदि) के लिए पानी में रहने के लिए पर्याप्त है। इसे जल विस्थापन विधि द्वारा भी एकत्र किया जा सकता है। मनुष्यों के लिए, ऑक्सीजन का सबसे महत्वपूर्ण गुण श्वसन और दहन का समर्थन करने की क्षमता है।
आप ऑक्सीजन कैसे प्राप्त कर सकते हैं?
प्रयोगशाला में, ऑक्सीजन युक्त ऑक्सीजन को गर्म करके ऑक्सीजन का उत्पादन किया जाता है
पोटेशियम परमैंगनेट, हाइड्रोजन पेरोक्साइड, पोटेशियम क्लोरेट जैसे पदार्थ। वे ऑक्सीजन की रिहाई के साथ विघटित होते हैं। निम्नलिखित समीकरणों पर ध्यान दें
हे
टी
2 मी एन के बारे में 4 → को 2 एम एन के बारे में 4 + एम एन के बारे में 2 + ओ 2
हे
टी, एमएनओ2
2 एच 2 ओ 2 → 2 एच 2 ओ + ओ 2
हे
टी
2KCLO 3 → 2KCL + 3O 2
इन समीकरणों में क्या समानता है?
सच कहा आपने। और ऐसी प्रतिक्रियाएं कहलाती हैंअपघटन प्रतिक्रियाएं. ये ऐसी अभिक्रियाएँ हैं जिनमें एक जटिल पदार्थ से कई सरल या जटिल पदार्थ प्राप्त होते हैं।
कृपया ध्यान दें कि हाइड्रोजन पेरोक्साइड की अपघटन प्रतिक्रिया में
प्रतिक्रियाओं के पाठ्यक्रम के लिए शर्तें, तापमान के अलावा, मैंगन सूत्र भी है (चतुर्थ) ऑक्साइड। यह पदार्थउत्प्रेरक कहा जाता है.
पृष्ठ 137 पर §17 में उत्प्रेरक कहलाने वाली परिभाषा खोजें। इस परिभाषा को अपनी कॉपी में लिखो।
उद्योग में, वे पदार्थ जो प्रकृति में व्यापक रूप से वितरित हैं, ऑक्सीजन का उत्पादन करने के लिए उपयोग किए जाते हैं।
यह पानी और हवा है।
पानी के माध्यम से एक प्रत्यक्ष धारा प्रवाहित की जाती है, और यह ऑक्सीजन की रिहाई के साथ विघटित हो जाती है।
तेज़। मौजूदा
2 एच 2 हे → 2 एच 2 + हे 2
- यह किस प्रकार की अभिक्रिया है ?
हवा से ऑक्सीजन छोड़ने के लिए, हवा को t º = -196ºС तक ठंडा किया जाता है। फिर तापमान बढ़ा दिया जाता है और तरल ऑक्सीजन घोल में रह जाती है। इसे विशेष जहाजों - ऑक्सीजन टैंकों में संग्रहित किया जाता है और उद्योग की जरूरतों के लिए उपयोग किया जाता है।
हम अगले पाठों में ऑक्सीजन के रासायनिक गुणों पर विचार करेंगे।
4. छात्रों के ज्ञान का संचार।
- पाठ में आपने क्या नया सीखा?
- रासायनिक तत्व ऑक्सीजन का वर्णन कीजिए।
- ऑक्सीजन के भौतिक गुणों का वर्णन कीजिए।
- व्याख्या करें कि प्रयोगशाला और उद्योग में ऑक्सीजन का उत्पादन कैसे किया जाता है।
- प्रतिक्रिया समीकरणों में गुणांकों को व्यवस्थित करें और विस्तार प्रतिक्रियाओं को खोजें।
Fe + HCL → FeCL 2 + H 2 CaCO 3 → CaO + CO 2
टीº
एन 2 ओ 5 → नहीं 2 + ओ 2 केबीआर + सीएल 2 → केसीएल + बीआर 2
टीº
पीबी + ओ 2 → पीबीओ केएनओ 3 → केएनओ 2 + ओ 2
5. पाठ के परिणाम।
ग्रेडिंग।
क्रिएटिव टीम को असाइनमेंट ऑक्सीजन की खोज के इतिहास पर एक रिपोर्ट तैयार करेगा।
6. होमवर्क।
2) एक आरेख बनाएं - सार
"ऑक्सीजन तत्व के लक्षण"
"ऑक्सीजन प्रयोगशाला और उद्योग का उत्पादन"
"ऑक्सीजन के भौतिक गुण"
3) ऑक्सीजन या इसके उपयोग के गुणों का वर्णन करते हुए एक सेनकान बनाने की कोशिश करें (पृष्ठ 12 देखें)।
पाठ 2
विषय।ऑक्सीजन के रासायनिक गुण: कोयला, सल्फर, फास्फोरस के साथ परस्पर क्रिया। कनेक्शन प्रतिक्रिया। ऑक्साइड, ऑक्सीकरण, दहन की अवधारणा।
पाठ मकसद: पाठ के दौरान, का एक विचार बनाना जारी रखें
"रासायनिक तत्व" और "सरल" की अवधारणाओं के बीच अंतर
पदार्थ";
विचार करना रासायनिक गुणएक साधारण पदार्थ
ऑक्सीजन;
समीकरण लिखने की क्षमता विकसित करना जारी रखें
रासायनिक प्रतिक्रिएं;
अवधारणाओं का परिचय दें: दहन प्रतिक्रिया, ऑक्साइड, ऑक्सीकरण, दहन;
सामान्यीकरण करने के लिए, मुख्य बात को उजागर करने की क्षमता बनाना जारी रखें।
कक्षाओं के दौरान।
संगठन। पल।
होमवर्क चेक करना।
ए) पूर्व कर रहा है। 9 (पृष्ठ 141)।
बी) तैयार की गई योजनाओं पर विचार करने के लिए - सार।
ग) कविता सुनना।
डी) रचनात्मक टीम से संदेश।
3. छात्रों के बुनियादी ज्ञान को अद्यतन करना।
- रासायनिक तत्व ऑक्सीजन किस सरल पदार्थ से बनता है?
- ऑक्सीजन कैसे एकत्रित किया जा सकता है? क्यों?
- आप कैसे सिद्ध कर सकते हैं कि कांच में ऑक्सीजन है?
- ऑक्सीजन के भौतिक गुणों की सूची बनाएं।
- उनमें से कौन मानव जीवन में महत्वपूर्ण भूमिका निभाते हैं? क्यों?
किसी पदार्थ के किन गुणों को रासायनिक कहा जाता है ?
4. नई सामग्री का अध्ययन।
ऑक्सीजन सबसे सक्रिय पदार्थों में से एक है; यह सरल पदार्थों के साथ प्रतिक्रिया करता है: धातु और अधातु, जटिल पदार्थों के साथ। गर्म होने पर अधिकांश प्रतिक्रियाएँ होती हैं।
आइए नजर डालते हैं ऐसी ही कुछ प्रतिक्रियाओं पर।
- ऑक्सीजन में सल्फर, कार्बन, अल्कोहल के दहन का प्रदर्शन।
आइए इन परिवर्तनों के समीकरण लिखें।
एस + हे 2 → इसलिए 2
चतुर्थ द्वितीय
सी + ओ 2 → सीओ 2
- §19 में लाल फॉस्फोरस जलाने के अनुभव का विवरण प्राप्त करें।
- हम फास्फोरस की दहन प्रतिक्रिया के लिए समीकरण लिखते हैं।
चतुर्थद्वितीय
4 पी + 5 हे 2 → 2 पी 2 हे 5
लिखित प्रतिक्रियाओं के समीकरणों में क्या सामान्य है।
- अभिक्रिया, जब अनेक यौगिकों से केवल एक ही जटिल पदार्थ प्राप्त होता है, कहलाती है कनेक्शन प्रतिक्रियाएं।
जिन अभिक्रियाओं में ऑक्सीजन शामिल होती है उन्हें अभिक्रियाएँ कहते हैं ऑक्सीकरण। यदि ऑक्सीकरण प्रक्रिया प्रकाश और गर्मी की रिहाई के साथ होती है, तो इसे कहा जाता हैजलता हुआ।
आइए उन यौगिकों को देखें जो सल्फर, कार्बन, फास्फोरस के दहन के दौरान बने थे।
- इन यौगिकों में क्या समानता है?
- लिखित सूत्रों में आप क्या अंतर देखते हैं:
इन यौगिकों को ऑक्साइड कहा जाता है।आक्साइड - ये जटिल पदार्थ हैं जिनमें दो तत्व होते हैं, जिनमें से एक ऑक्सीजन है।
इस पाठ में हमने जो कुछ भी नया सीखा है, उसे संक्षिप्त आरेख के रूप में लिखा जा सकता है।
![]() मुझेऑक्सीकरण
मुझेऑक्सीकरण
हे2 + नहींमुझेइ 2 के बारे मेंएक्स
एसएल। इन-वादहन आक्साइड।
5. छात्रों के ज्ञान का समेकन।
- पाठ में हमने क्या नया सीखा?
आपको पाठ के बारे में क्या पसंद आया?
आपको क्या पसंद नहीं आया?
आपको कौन सा छात्र सबसे अधिक सक्रिय लगता है?
- पदार्थों की सूची में से ऑक्साइड के सूत्र लिखिए
HNO 3, K 2 O, NaCl, HJ, CaO, H 2 So 4, So 2, CuSo 4, O 2।
- निम्नलिखित प्रतिक्रियाओं के समीकरणों में गुणांकों को व्यवस्थित करें।
फ़े+ओ2 → फे3 हे4 सीए + हे2 → काओ
एसओ 2 + ओ 2 → एसओ 3 ली + ओ 2 → ली 2 ओ
एच 2 + ओ 2 → एच 2 ओ पीएच 3 + ओ 2
केएमएनओ 4 हे 2
बाओ
रासायनिक तत्व ऑक्सीजन दो अलॉट्रोपिक संशोधनों के रूप में मौजूद हो सकता है, अर्थात दो सरल पदार्थ बनाता है। इन दोनों पदार्थों में आणविक संरचना होती है। उनमें से एक का सूत्र O 2 है और इसे ऑक्सीजन कहा जाता है, अर्थात। रासायनिक तत्व के नाम के समान जिसके साथ यह बनता है।
ऑक्सीजन द्वारा निर्मित एक अन्य सरल पदार्थ को ओजोन कहा जाता है। ओजोन, ऑक्सीजन के विपरीत, त्रिकोणीय अणु होते हैं, अर्थात। इसका सूत्र O3 है।
चूँकि ऑक्सीजन का मुख्य और सबसे सामान्य रूप आणविक ऑक्सीजन O2 है, इसलिए हम पहले इसके रासायनिक गुणों पर विचार करेंगे।
रासायनिक तत्व ऑक्सीजन सभी तत्वों के बीच वैद्युतीयऋणात्मकता के मामले में दूसरे स्थान पर है और फ्लोरीन के बाद दूसरे स्थान पर है। इस संबंध में, ऑक्सीजन की उच्च गतिविधि और इसमें लगभग विशेष रूप से ऑक्सीकरण गुणों की उपस्थिति को मानना तर्कसंगत है। वास्तव में, सरल और जटिल पदार्थों की सूची जिनके साथ ऑक्सीजन प्रतिक्रिया कर सकता है, बहुत बड़ी है। हालांकि, यह ध्यान दिया जाना चाहिए कि चूंकि ऑक्सीजन अणु में एक मजबूत दोहरा बंधन होता है, ऑक्सीजन के साथ अधिकांश प्रतिक्रियाओं में गर्मी के उपयोग की आवश्यकता होती है। अक्सर, प्रतिक्रिया (इग्निशन) की शुरुआत में मजबूत हीटिंग की आवश्यकता होती है, जिसके बाद बाहर से गर्मी की आपूर्ति के बिना कई प्रतिक्रियाएं स्वतंत्र रूप से आगे बढ़ती हैं।
सरल पदार्थों में केवल ऑक्सीजन द्वारा ऑक्सीकरण नहीं किया जाता है कीमती धातु(Ag, Pt, Au), हैलोजन और अक्रिय गैसें।
सल्फर ऑक्सीजन में जलकर सल्फर डाइऑक्साइड बनाता है:
फास्फोरस, ऑक्सीजन की अधिकता या कमी के आधार पर, फास्फोरस (V) ऑक्साइड और फास्फोरस (III) ऑक्साइड दोनों बना सकता है:
नाइट्रोजन के साथ ऑक्सीजन की परस्पर क्रिया अत्यंत कठोर परिस्थितियों में होती है, क्योंकि ऑक्सीजन और विशेष रूप से नाइट्रोजन अणुओं में बाध्यकारी ऊर्जा बहुत अधिक होती है। दोनों तत्वों की उच्च वैद्युतीयऋणात्मकता भी प्रतिक्रिया की जटिलता में योगदान करती है। प्रतिक्रिया केवल 2000 o C से ऊपर के तापमान पर शुरू होती है और प्रतिवर्ती होती है:
ऑक्साइड बनाने के लिए सभी साधारण पदार्थ ऑक्सीजन के साथ प्रतिक्रिया नहीं करते हैं। इसलिए, उदाहरण के लिए, सोडियम, ऑक्सीजन में जलकर, एक पेरोक्साइड बनाता है:
और पोटेशियम सुपरऑक्साइड है:
अक्सर, जब जटिल पदार्थों को ऑक्सीजन में जलाया जाता है, तो मूल पदार्थ बनाने वाले तत्वों के आक्साइड का मिश्रण बनता है। उदाहरण के लिए:
हालांकि, ऑक्सीजन में दहन के दौरान, नाइट्रोजन युक्त कार्बनिक पदार्थनाइट्रिक ऑक्साइड के स्थान पर आण्विक नाइट्रोजन N2 बनता है। उदाहरण के लिए:
जब क्लोरीन डेरिवेटिव को ऑक्सीजन में जलाया जाता है, तो क्लोरीन ऑक्साइड के बजाय हाइड्रोजन क्लोराइड बनता है:
ओजोन के रासायनिक गुण:
ओजोन ऑक्सीजन की तुलना में एक मजबूत ऑक्सीकरण एजेंट है। यह इस तथ्य के कारण है कि ओजोन अणु में ऑक्सीजन-ऑक्सीजन बंधनों में से एक आसानी से टूट जाता है और इसके परिणामस्वरूप अत्यंत सक्रिय परमाणु ऑक्सीजन बनता है। ओजोन, ऑक्सीजन के विपरीत, अपने उच्च ऑक्सीकरण गुणों को प्रकट करने के लिए हीटिंग की आवश्यकता नहीं होती है। यह सामान्य और कम तापमान पर भी अपनी गतिविधि दिखाता है:
पीबीएस + 4 ओ 3 \u003d पीबीएसओ 4 + 4 ओ 2
जैसा ऊपर बताया गया है, चांदी ऑक्सीजन के साथ प्रतिक्रिया नहीं करती है, हालांकि, यह ओजोन के साथ प्रतिक्रिया करती है:
2Ag + O 3 \u003d Ag 2 O + O 2
ओजोन की उपस्थिति के लिए एक गुणात्मक प्रतिक्रिया यह है कि जब परीक्षण गैस को पोटेशियम आयोडाइड के घोल से गुजारा जाता है, तो आयोडीन का बनना देखा जाता है:
2KI + O 3 + H 2 O = I 2 ↓ + O 2 + 2KOH
सल्फर के रासायनिक गुण
एक रासायनिक तत्व के रूप में सल्फर कई एलोट्रोपिक संशोधनों में मौजूद हो सकता है। रोम्बिक, मोनोक्लिनिक और प्लास्टिक सल्फर के बीच अंतर करें। मोनोकलिनिक सल्फर को रम्बिक सल्फर मेल्ट की धीमी गति से ठंडा करके प्राप्त किया जा सकता है, जबकि प्लास्टिक, इसके विपरीत, एक सल्फर मेल्ट को तेज ठंडा करके प्राप्त किया जाता है जिसे पहले उबाला गया हो। प्लास्टिक सल्फर में अकार्बनिक पदार्थों के लिए लोच की एक दुर्लभ संपत्ति होती है - यह बाहरी बल की क्रिया के तहत विपरीत रूप से खिंचाव करने में सक्षम होता है, जब यह प्रभाव समाप्त हो जाता है तो यह अपने मूल रूप में लौट आता है। रंबिक सल्फर सामान्य परिस्थितियों में सबसे अधिक स्थिर है, और अन्य सभी अलॉट्रोपिक संशोधन समय के साथ इसमें गुजरते हैं।
रम्बिक सल्फर के अणुओं में आठ परमाणु होते हैं, अर्थात इसका सूत्र S8 के रूप में लिखा जा सकता है। हालांकि, चूंकि सभी संशोधनों के रासायनिक गुण काफी समान हैं, ताकि प्रतिक्रिया समीकरणों को लिखना मुश्किल न हो, किसी भी सल्फर को प्रतीक एस द्वारा निरूपित किया जाता है।
सल्फर सरल और जटिल दोनों पदार्थों के साथ परस्पर क्रिया कर सकता है। रासायनिक प्रतिक्रियाओं में, यह ऑक्सीकरण और कम करने वाले गुणों दोनों को प्रदर्शित करता है।
सल्फर के ऑक्सीकरण गुण तब प्रकट होते हैं जब यह धातुओं के साथ-साथ कम विद्युतीय तत्व (हाइड्रोजन, कार्बन, फास्फोरस) के परमाणुओं द्वारा गठित गैर-धातुओं के साथ संपर्क करता है:
कम करने वाले एजेंट के रूप में, सल्फर अधिक विद्युतीय तत्वों (ऑक्सीजन, हैलोजेन) द्वारा गठित गैर-धातुओं के साथ-साथ एक स्पष्ट ऑक्सीकरण समारोह के साथ जटिल पदार्थों के साथ बातचीत करता है, उदाहरण के लिए, केंद्रित सल्फ्यूरिक और नाइट्रिक एसिड:
उबलने के दौरान सल्फर भी केंद्रित के साथ बातचीत करता है जलीय समाधानक्षार। अंतःक्रिया असमानता के प्रकार के अनुसार आगे बढ़ती है, अर्थात सल्फर दोनों कम करता है और इसके ऑक्सीकरण राज्य को बढ़ाता है।